بروميد الفضة
من ويكيبيديا،
| بروميد الفضة | |
|---|---|
| أسماء أخرى | |
| bromargyrite bromyrite silver(I) bromide | |
| المعرفات | |
| رقم CAS | 7785-23-1 |
| بوب كيم | 66199 |
| مواصفات الإدخال النصي المبسط للجزيئات˂ | |
| المعرف الكيميائي الدولي˂ | |
| الخواص | |
| الصيغة الجزيئية | AgBr |
| الكتلة المولية | 187.77 غ/مول |
| المظهر | صلب أصفر شاحب |
| الكثافة | 6.47 غ/سم3 |
| نقطة الانصهار | 430 °س |
| نقطة الغليان | 1502 °س |
| الذوبانية في الماء | غير منحل عملياً |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري – تعديل |
بروميد الفضة هو مركب كيميائي صيغته AgBr، ويوجد في الشروط القياسية على شكل صلب بلوري أصفر شاحب اللون.
الوفرة الطبيعية والتحضير
يوجد بروميد الفضة في الطبيعة على شكل معدن برومارجيريت.
يمكن تحضير المركب مخبرياً من تفاعل ترسيب بعملية مزج نترات الفضة مع بروميد البوتاسيوم: A g N O 3 + K B r ⟶ A g B r ↓ + K N O 3 {\displaystyle \mathrm {AgNO_{3}+KBr\longrightarrow AgBr\downarrow +\ KNO_{3}} }
الخواص
يوجد بروميد الفضة في الشروط القياسية على شكل صلب بلوري له لون أصفر شاحب، حساس للضوء؛ وهو عملياً غير منحل في الماء (ينحل منه مجرد 0.14 ميليغرام في الليتر عند 25°س.
)
الاستخدامات
نظراً للحساسية الضوئية لمركب بروميد الفضة لذلك استخدم في التصوير الفوتوغرافي منذ القرن التاسع عشر
ــــــــ

بروميد الفضة (AgBr): التركيب والتوليف والخصائص والاستخدامات
بروميد الفضة هو ملح غير عضوي تركيبة كيميائية له هي AgBr. يتكون صلتها من Ag + الكاتيونات والنباتات بنسبة 1: 1 ، التي تجذبها القوى الإلكتروستاتيكية أو الروابط الأيونية. يمكن أن نرى كما لو أن الفضة المعدنية أعطت واحدة من إلكترونات التكافؤ إلى البروم الجزيئي.
تشبه طبيعتها كلوريد “الإخوة” ويوديد الفضة. الأملاح الثلاثة غير قابلة للذوبان في الماء ، ولها ألوان مماثلة ، وبالإضافة إلى ذلك ، حساسة للضوء. أي أنهم يعانون من التفاعلات الكيميائية الضوئية. تم استخدام هذه الخاصية للحصول على صور فوتوغرافية ، نتيجة لتخفيض أيونات Ag + إلى الفضة المعدنية.
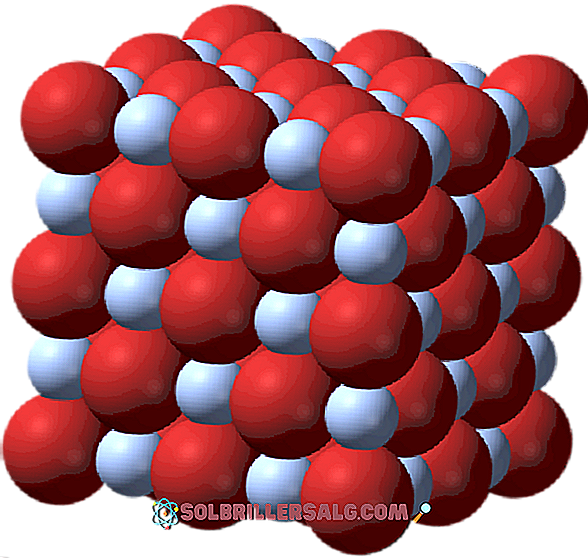
في الصورة العليا ، يظهر الزوج الأيوني Ag + Br- ، حيث تتوافق المجالات البيضاء والبنية مع Ag + و Brions ، على التوالي. هنا يمثلون الرابطة الأيونية مثل Ag-Br ، لكن من الضروري الإشارة إلى أنه لا يوجد رابط تساهمي بين كلا الأيونيين.
قد يبدو متناقضا بالنسبة للفضة للمساهمة اللون الأسود للصور عديمة اللون. وذلك لأن AgBr يتفاعل مع الضوء ، مما يولد صورة كامنة ؛ الذي ، ثم ، يكثف عن طريق زيادة الحد من الفضة.
هيكل بروميد الفضة
أعلاه لديك شبكة أو هيكل الكريستال من بروميد الفضة. يتم عرض تمثيل أكثر دقة لفرق الحجم بين نصف قطر أيون Ag + و Br- هنا. تغادر أكبر عدد من المناطق الصغيرة حيث تتواجد Ag + cations ، وهو محاط بستة Br- (والعكس بالعكس).
هذا الهيكل هو سمة من سمات نظام بلوري مكعب ، وتحديدا من نوع الملح الصخري. نفس الشيء ، على سبيل المثال ، بالنسبة لكلوريد الصوديوم ، NaCl. في الواقع ، فإن الصورة تسهل ذلك من خلال توفير حد مكعب مثالي.
للوهلة الأولى ، تجدر الإشارة إلى أن هناك بعض الاختلاف في الحجم بين الأيونات. هذا ، وربما الخصائص الإلكترونية لل Ag + (والتأثير المحتمل لبعض الشوائب) ، يؤدي إلى وجود عيوب في بلورات AgBr ؛ وهذا يعني ، الأماكن التي يتم فيها كسر تسلسل ترتيب الأيونات في الفضاء.
عيوب الكريستال
تتكون هذه العيوب من فراغات تركتها أيونات مفقودة أو نازحة. على سبيل المثال ، بين ستة أنونات Br ، يجب أن يكون Ag + cation موجودًا عادةً ؛ ولكن بدلاً من ذلك ، قد يكون هناك فراغ لأن الفضة انتقلت إلى فجوة أخرى (عيب Frenkel).
على الرغم من أنها تؤثر على الشبكة البلورية ، إلا أنها تفضل تفاعلات الفضة مع الضوء ؛ وكلما زاد حجم البلورات أو الكتلة (حجم الحبوب) ، زاد عدد العيوب ، وبالتالي ، سيكون أكثر حساسية للضوء. أيضًا ، تؤثر الشوائب على الهيكل وهذه الخاصية ، خاصة تلك التي يمكن تقليلها باستخدام الإلكترونات.
نتيجة لهذا الأخير ، تتطلب بلورات AgBr الكبيرة تقليل التعرض للضوء ؛ وهذا هو ، فهي أكثر من المرغوب فيه لأغراض التصوير الفوتوغرافي.
تركيب
في المختبر ، يمكن تصنيع بروميد الفضة عن طريق خلط محلول مائي من نترات الفضة ، AgNO 3 ، مع بروميد الصوديوم الملحي ، NaBr. الملح الأول يساهم بالفضة ، والثاني البروميد. فيما يلي تفاعل الإزاحة المزدوجة أو الميثازيس الذي يمكن تمثيله بالمعادلة الكيميائية أدناه:
AgNO 3 (aq) + NaBr (s) => NaNO 3 (aq) + AgBr (s)
لاحظ أن ملح نترات الصوديوم ، NaNO 3 ، قابل للذوبان في الماء ، بينما يترسب AgBr كمادة صلبة بلون أصفر باهت. بعد ذلك يتم غسل المادة الصلبة وتعريضها لتجفيف الفراغ. بالإضافة إلى NaBr ، يمكن أيضًا استخدام KBr كمصدر للأنيونات البروميد.
من ناحية أخرى ، يمكن الحصول على AgBr بشكل طبيعي من خلال البرومريت المعدني وعمليات التنقية اللازمة.
خصائص
مظهر
الأصفر البياض الصلبة مثل الطين.
الكتلة الجزيئية
187.77 جم / مول.
كثافة
6.473 جم / مل.
نقطة انصهار
432 درجة مئوية
نقطة الغليان
1502 درجة مئوية
الذوبان في الماء
0.140 جم / مل عند 20 درجة مئوية
معامل الانكسار
2253.
القدرة الحرارية
270 J / Kg · K.
حساسية للضوء
قيل في القسم السابق أن هناك عيوبًا في بلورات AgBr تعزز حساسية هذا الملح للضوء ، لأنها تحبس الإلكترونات المتكونة ؛ وبالتالي ، من الناحية النظرية ، يتم منعهم من التفاعل مع الأنواع الأخرى في البيئة ، مثل الأكسجين من الهواء.
يتم تحرير الإلكترون من ردة الفعل مع الفوتون:
Br- + hv => 1 / 2Br 2 + e-
لاحظ أنه يتم إنتاج Br 2 ، مما يؤدي إلى تلطيخ اللون الأحمر الصلب إذا لم يتم إزالته. تقلل الإلكترونات التي تم إصدارها من الكاتيونات Ag + ، في فتراتها الفاصلة ، إلى الفضة المعدنية (تُمثل أحيانًا باسم Ag0):
Ag + + e- => Ag
وبعد ذلك المعادلة الصافية:
AgBr => Ag + 1 / 2Br 2
عندما يتم تشكيل “الطبقات الأولى” من الفضة المعدنية على السطح ، يقال أن هناك صورة كامنة ، لا تزال غير مرئية للعين البشرية. تصبح هذه الصورة مرئية بملايين المرات إذا زادت الأنواع الكيميائية الأخرى (مثل الهيدروكينون والفيون ، في عملية التطوير) من تقليل بلورات AgBr إلى الفضة المعدنية
تطبيقات

بروميد الفضة هو الأكثر استخدامًا في جميع هاليداته في مجال كشف الأفلام الفوتوغرافية. يتم تطبيق AgBr على الأفلام المذكورة ، المصنوعة من خلات السليلوز ، مع وقف التنفيذ في الجيلاتين (مستحلب التصوير الفوتوغرافي) ، وفي وجود 4- (ميثيلامينو) سلفات الفينول (ميتول) أو فييدون ، وهيدروكينون.
مع كل هذه الكواشف ، يمكنك إعطاء الحياة للصورة الكامنة. إنهاء وتسريع تحويل الفضة الأيونية إلى المعدنية. لكن إذا لم تمضِ بعناية وعناية معينة ، فسوف تصدأ جميع الفضة على السطح ، وينتهي التباين بين اللونين الأسود والأبيض.
هذا هو السبب في أن خطوات التوقف والاستحمام والغسيل للأفلام الفوتوغرافية تعتبر حيوية.
هناك فنانين يلعبون بهذه العمليات بطريقة يخلقون بها فروق دقيقة من الألوان الرمادية التي تثري جمال الصورة وإرثها ؛ وكل هذا يفعلونه ، ربما في بعض الأحيان دون الشك في ذلك ، وذلك بفضل التفاعلات الكيميائية ، التي يمكن أن يكون أساسها النظري معقدًا بعض الشيء ، وأغبر حساس للضوء يمثل نقطة انطلاق.