مطياف
من ويكيبيديا،

مطياف بسيط
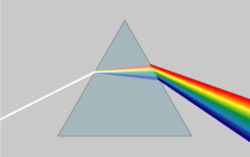
انكسار شعاع ضوء في المنشور.
المطياف في الفيزياء والكيمياء هو جهاز يستعمل لقياس الخواص الضوئية عبر نطاق معين من طيف الموجات الكهرومغناطيسية، وبصفة خاصة يقوم بالتحليل الضوئي للتعرف على مكونات المواد.
وقد تقاس مباشرة شدة الضوء أو استقطاب الضوء. وهو يقوم بقياس طول الموجات الضوئية حيث تتناسب طول الموجة تناسبا عكسيا مع طاقة الفوتون. ويمكن كتابة طاقة الفوتون أو طاقة شعاع الضوء بوحدة إلكترون فولت، وعادة يعبر عن طاقة شعاع الضوء بطول الموجة، أي بوحدة نانومتر.
ويستعمل المطياف لإنتاج التحليل الطيفي الذي يظهر في هيئة خطوط ضوئية ملونة نظرا لاختلاف طول الموجة لكل خط عن الآخر. ويمكن بمعرفة مجموعة الخطوط الضوئية الناتجة عن مادة معينة تعيين انوع لمادة بدقة ،لأن كل عنصر كيميائي يتميز ببصمة خاصة به (أي بطيف معين خاص به).
ويستخدم التعبير مطياف للتعريف عن الأجهزة التي تقوم بقياس طول موجة الأشعة في نطاق واسع من طول الموجة، من أشعة غاما ذات طول الموجة القصيرة جدا إلى منطقة الأشعة السينية إلى منطقة الضوء المرئيذات طول موجة متوسطة الطول، إلى نطاق الأشعة تحت الحمراء ذات الموجات الطويلة. وإذا كانت منطقة الدراسة محصورة في منطقة الضوء المرئي فيسمى المطياف المطياف البصري.
وفي منطقة الموجات الكهرومغناطيسية التي تكون تحت الطيف المرئي مثل الميكروويف والموجات الراديوية فإن جهاز تحليل الطيف يصبح جهازا إلكترونيا بحتا، مثل الراديو (ليس ضوئيا).
تركيب المطياف:

مطياف بسيط
يتكون المطياف الضوئي البسيط من الأجزاء الآتية:
- S مصدر الضوء المطلوب تعيين طيفه
- ينفذ شعاع المصدر خلال فتحة رأسية ضيقة F1 من أجل تكوين شعاعا ساقطا أشعته متوازية يسقط على العدسة L1
- موشور زجاجي P لكسر الشعاع المطلوب تحليله،
- تخرج الأشعة من الموشور محللة (منفصلة) طبقا للونها وتسقط على عدسة ثانية L2 لتخرج من عدسة مخرج المطياف (عند العين)،
- عدسة خروج الأشعة تمكن من رؤية خطوط الطيف بالعين وقياسها. كما يمكن الاستعاضة عنها بوضع عدسة ثالثة في طريق الأشعة واستقبال الإشعة على حائل أو مقياس ضوئي.
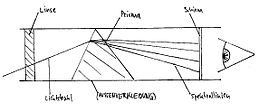
بغرض قياس الزوايا بين خطوط الطيف الناشئة تكون العدسة L2 للتلسكوب متحركة ومتكئة على مقياس معلم لأخذ القراءة مباشرة عليه.
مقاييس الطيف
تعطي المطيافات الحديثة الطيف بصفة عامة (في نطاق الأشعة فوق البنفسجية والضوء المرئي والأشعة تحت الحمراء بالوحدات الأتية : طول الموجة بوحدة نانو متر nm، عدد الموجات/متر um-1 أو إلكترون فولت eV.

طيف ضوء لمبة الزئبق. تبين الصورة السفلى خطوط الطيف المميزة للزئبق. ويبين الشكل العلوي طول الموجة بالنانومتر (المحور الأفقي)، وشدة الضوء (المحور الرأسي).
وكما نستخلص من الشكل فاللون البنفسجي للضوء له طول موجة 8و435 نانومتر ،واللون الأخضر له طول موجة 546 نانومتر، كما يوجد في الطيف خطوط أخرى.
أنواع أخرى للمطياف
توجد لأشعة الجسيمات طريقة مطيافية الكتلة حيث تستغل القوة المركزية الطاردة للتفرقة بين الجسيمات الثقيلة والخفيفة. كما تستغل تأثيرات فيزيائية أخرى ،مثل تأثير شتارك الذي يعتمد على استخدام مجال كهربائي لفصل خطوط الطيف القادمة من المصدر. كذلك توجد مطيافات تعمل بالمجال المغناطيسي لفصل خطوط الطيف وهي تعتمد في نظريتها على تأثير زيمان. أما في حالة الجسيمات الثقيلة وفي حالة الجسيمات المتهادلة الشحنة مثل النيوترونات فيستخدم المطياف المسمى مطياف زمن الطيران وهو يمكنه قياس فروق السرعات للجسيمات.
بالنسبة إلى طريقة تحليل سرعات جسيمات فطريقة مطياف زمن الطيران تعتمد على أنه إذا انطلقت الجسيمات في الزمن to وبدأنا القياس على بعد 20 متر مثلا من فتحة انطلاق الجسيمات لوجدنا أن الجسيم السريع يصل عدادنا أولا عند الزمن t1. أما الجسيم البطيئ فهو يصل العداد متأخرا في الزمن t2. هذه هي فكرة قياس زمن طيران الجسيمات لتعيين سرعاتها المختلفة، وهي عملية تحليل السرعات، وتطبق كثيرا في تجارب فيزياء الجسيمات.
مطيافية
من ويكيبيديا،
المطيافية منظار الطيف
(Spectroscopy) هي علم التآثر بين الإشعاع (سواء كان كهرومغناطيسيا أو إشعاع جسيمات) مع المادة والتي تشمل الذرات والجزيئات.
أما قياس الطيف (القياسات الطيفية) فهو قياس هذه التآثرات الناتجة عن عملية امتصاص شعاع كهرومغناطيسي أو انبعاث شعاع كهرومغناطيسي أو تبعثر (تشتت ) للطيف الكهرومغناطيسي ، والأجهزة التي تقوم بهذه القياسات التي تدعى مطياف أو راسم طيفي.

الضوء الأبيض يتكون من طيف مركب مختلف الألوان.
تصدر المادة طيفا عند امتصاصها لطاقة ؛ فمثلا إذا قمنا بتسخين قطعة من الحديد فإنها تحمر أولا ُم يتغير لونها بارتفاع درجة الحرارة فتصبح برتقالية اللون، وإذا زادت درجة حرارتها فيميل وميضها إلى الاصفرار. كل هذا يسمى طيفا . وكذلك يمكنك التسبب في احمرار قطعة الحديد إذا ما قمت بطرقها بمطرقة مع مواصلة عملية الطرق حتى تحمر، ذلك لأنها تمتص جزءا من طاقة الطرق (طاقة الحركة) وتحوله إلى حرارة وتلك الحرارة تجعلها تصدر وميضا هو الطيف.
إذا قمنا بتحليل طيف قطعة الحديد وصورناه على فيلم تصوير فإننا نجده مكون من خطوط من الضوء متوازية متراصة بين خطوط حمراء فخطوط برتقالي فخطوط صفراء، هذا هو طيف قطعة الحديد الساخنة ؛ ويظهر في هيئة خطوط ضوئية لونية لأنها تمثل انتقالات لإلكترونات الحديد بين مستويات الطاقة المختلفة للإلكترونات في ذرة الحديد، وعند انتقال إلكترون من مستوى طاقة في الذرة عالي إلى مستوى طاقة منخفض فهو يصدر شعاع ضوء له طاقة تعادل الفرق بين طاقتي المستويين في الذرة .
كذلك عندما نقوم بتسخين قطعة من النحاس فهي تصدر أيضا طيفا ضوئيا، ولكن خطوط طيفها تكون مختلفة عن خطوط طيف قطعة الحديد الساخن ( اختلاف في أطوال الموجات الضوئية الصادرة (فوتونات)) بسبب اختلاف البنية الإلكترونية الذرية في المادتين . فمن طيف الحديد نتعرف على الحديد ومن طيف النحاس نتعرف على النحاس . والجهاز الذي يقوم بتحليل تلك الأطياف ويظهر خطوطها يسمى مطياف.
بجهاز المطياف يمكننا التعرف على المواد عن طريق تحليل أطيافها .
كيف ينشأ الطيف
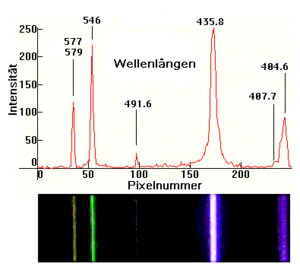
طيف مصباح الزئبق ، صورته آلة تصوير خلف موشور. (عدد البكسلات يتناسب مع طول موجة شعاع الضوء)
سنأخذ مثال الطيف الضوئي الذي نعرفه لضوء الشمس. تحتوي الشمس في معظمها على عنصر الهيدروجين . هذا الهيدروجين في درجات حرارة عالية بحيث يقفز إلكترون ذرة الهيدروجين إلى مستوى طاقة عالية في ذرة الهيدروجين. أي أن الإلكترون يكون مثارا أو ذرة الهيدروجين تكون مثارة بحيث أن ذرة الهيدروجين لا تستطيع البقاء مثارة طوال الوقت ؛ فبعد فترة وجيزة يعود الإلكترون إلى مستواه الأرضي – إلى مستوى طاقة أقل – بعدما يتخلص من جزء من الطاقة التي تسببت في إثارته. تلك الطاقة التي يتخلص منها هي الفرق بين طاقته أثناء الإثارة وطاقة بعد هبوطه إلى مستوى طاقة أقل في ذرة الهيدروجين. ويطلق تلك الطاقة في هيئة شعاع ضوء . ويكون لدى شعاع الضوء تردد متناسبا مع طاقتة . أي إذا كانت طاقة الشعاع عالية كان تردد موجته عالية، وإذا كانت طاقة الشعاع منخفضة يكون تردد موجة الشعاع منخفضة.
قد يعود إلكترون ذرة الهيدروجين من مستوى طاقة رقم 5 إلى مستوي تحته مثالا إلى مستوي طاقة رقم 3 ؛ أو قد يعود إلى مستوى طاقة رقم 2 ألو إلى المستوي الأرضي رقم 1. في كل تلك الحالات تختلف كمية الطاقة التي تصدر من كل قفزة من تلك القفزات عن الأخرى، وتبدو كخطوط طيف على حائل عندما تنكسر على موشور .
إذا قمنا في المعمل بتسخين الصوديوم مثلا إلى درجة عالية نجد أنه يشع ضوءا أصفرا برتقاليا، وإذا قمنا بتحليل طيفه هذا لوجدنا أن له خطوطا طيف تختلف عن خطوط طيف الهيدروجين. الاختلاف يظهر كاختلاف في ترددات الأشعة الصادرة من الصوديوم عن ترددات الاشعة الصادرة من الهيدروجين. فكل عنصر كيميائي له بصمة هي طيفه ؛ ويمكن التعرف على العنصر من طيفه (بصمته).
وطيف عنصر يمكن رسمه في رسم بياني يعطي العلاقة بين شدة خطوط الطيف و وتردداتها ، أو طول موجة خط الطيف. والعلاقة بين تردد شعاع ضوء (موجة كهرومغناطيسية) ν {\displaystyle \nu \,} 



أساس فهمنا لتكوين الطيف يعود إلى نموذج بور لذرة الهيدروجين . وبواسطة هذا النموذج يمكن تفسير امتصاص الذرة وإصدارها فوتونات (أشعة ضوئية) عند انتقال الإلكترون بين مستويات الطاقة المختلفة في الذرات . الطاقة الممتصة وبالتالي الطاقة الصادرة Δ E {\displaystyle \Delta E\,} 


وتنطبق عليها المعادلة: Δ E = E n − E m = h ⋅ ν {\displaystyle \Delta E=E_{n}-E_{m}=h\cdot \nu \,}
وعندما يكون الفرق E n > E m {\displaystyle E_{n}>E_{m}\,} 
وبنيات كل طيف تشير إلى الطاقات المختلفة التي يستطيع عنصر امتصاصها أو إشعاعها (إصدارها). كميات الطاقة هذه تعادل الفرق بين طاقات المستويات المختلفة في العينة. ويعتمد طيف عنصر ما على تركيزه في العينة وعلى الانتقالات المسموحة لانتقال الإلكترون فيه.
استخداماتها

تحليل الضوء الأبيض بواسطة المنشور إلى ألوان هو مثال على المطيافية

موقع حيز الطيف المرئي في طيف الموجات الكهرومغناطيسية في الوسط في حيز ضيق . أشد الأشعة طاقة هي أشعة غاما (يسار). الترقيم العلوي يعطي تردد الشعاع بالهرتز والترقيم السفلي للطيف الكلي يعطي طول الموجة بالمتر.
تاريخيا، أشير للمطيافية على أنها أحد فروع العلوم الذي يستخدم فيه الضوء المرئي لدراسة بنيات المادة و للتحليل النوعي والكمي لها. وكان نصرا كبيرا عند معرفة مكونات الشمس من مجرد تحليل طيف ضوئها، ونحن هنا على الأرض، فنعرف أنها في معظمها تتكون من الهيدروجين مع قليل من الهيليوم (نحو 4% )وقليل من الليثيوم (أقل من 1% ) . (يوجد في قلب الشمس أيضا الحديد والعناصر الأخرى كالكربون والأكسجين والنتروجين وغيرها بنسبة صغيرة ولكن الحديد على الأخص لا يظهر على السطح . سطح الشمس هو الذي يصدر الضوء الذي نتلقاه منها وهو مكون من الهيدروجين والهيليوم والليثيوم). كان ذلك نصرا عظيما للمطيافية. وبتطبيق الطريقة على النجوم وجدنا أن أغلبها يماثل الشمس في تكوينها وطيفها ؛ إلا أن للنجوم أجيال وأجيال ولهذا تختلف أطيافها عن طيف الشمس . وهذا الموضوع له متخصصيه في علم الفلك .
ثم تم توسيع تعريف المطيافية بعد إدخال وتطوير تقنيات جديدة لإنتاج الأشعة، مثل الأشعة السينية والأشعة الراديوية وأشعة الرادار واكتشفنا أشعة غاما التي تصدرها بعض الذرات . واتضح لنا أن الطيف أعرض بكثير من الحيز الضيق الذي نسمية الطيف المرئي ؛ فكلها أنواع من الأشعة الكهرومغناطيسية ولكنها تختلف فيما تحمله من طاقة . أشدها طاقة هي أشعة غاما.
المطيافية تسخدم غالبا في الكيمياء الفيزيائية والتحليلية للتحليل النوعي والكمي للمواد الكيميائية سواء كانت ذرية باستخدام الاطياف الذرية لتلك العناصر أو لتحليل الجزيئات . يتم ذلك بتسليط الأشعة المرئية على العينة أو أشعة فوق البنفسجية أو أشعة تحت الحمراء للتفاعل معها، اذ تمتص منها بعض ذرات العنصر، وقياس ما يصدر منها من ضوء أو موجات كهرومغناطيسية . وابتكرت أنواع مختلفة من المطيافات ، فمنها مطيافية الأشعة فوق البنفسجية ومطيافية الأشعة تحت الحمراء ومطيافية إلكترون أوجيه ، ومطيافية الانبعاث الضوئي ، وغيرها .
وابتكرت أنواع تستخدم أيضا بكثرة في علم الفلك والاستشعار عن بعد . تزود التلسكوبات الكبيرة دوما بمطياف أو مطيافات مختلفة لقياس إما التركيب الكيميائي أو الخواص الفيزيائية للأجرام الفلكية أو قياس السرعات حسب انزياح دوبلر لخطوطهم الطيفية.